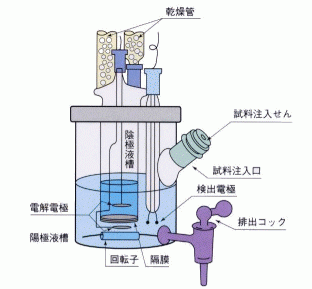
カールフィッシャー水分測定装置(水分計)
カールフィッシャー水分測定方法 電量滴定法
概要
水分は、固体・液体・気体の持っている含水質量の百分率で表されます。
水分の測定方法には、カールフィッシャー法・乾燥法・赤外線吸収法・誘電率法などがあり、これらのうち主としてカールフィッシャー法と乾燥法が実験室で用いられています。
弊社の装置ではカールフィッシャー法を採用しています。カールフィッシャー法による水分測定法は、滴定セル内でヨウ化物イオン・二酸化硫黄・アルコールを主成分とする電解液(カールフィッシャー試薬(以下KF試薬))が、メタノールの存在下で水と特異的に反応することを利用して、物質中の水分を定量するものです。この方法は、滴定の取り進め方により、電量法と容量法に分けられます。電量滴定法は、検出感度が非常に高く、定量範囲が数μg~30 mgH2O までの測定が理論上可能です。
測定原理
カールフィッシャー反応
水は塩基とアルコールの存在下でヨウ素、二酸化硫黄と反応します。
H2O+I2+SO2+CH3OH+3RN → 2RN・HI+RN・HSO4CH3…(1)
電量滴定法
ヨウ化物イオンを含む電解液(陽極液)中で電解により、陽極にてヨウ化物イオンからヨウ素を発生させます。
2I- - 2e → I2…(2)
(2) 式で発生したヨウ素が (1) 式に従って消費されると、検出電極でヨウ素が消費されたことを検出し、再び電解により (2) 式に従って陽極からヨウ素を発生させます。発生するヨウ素は『ファラデーの法則』に従って電気量に比例します。
(1)式より、H2OとI2は1:1の反応であることから、水1モル(18.02g)は2×96485クーロンに相当します。 従って水1mgは10.71クーロンに相当します。
以上の原理に基づき、電解に要した電気量より、水分量を換算します。